|
|
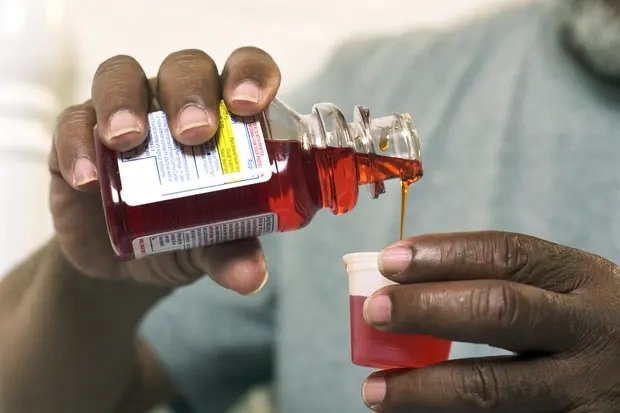
4 mẫu siro liên quan cái chết của hàng chục trẻ tại Gambia đều do Maiden Pharmaceuticals (Ấn Độ) sản xuất. Ảnh: Guardian. |
Theo Bộ Y tế Ấn Độ, cơ quan này đang kiểm tra các mẫu siro ho do Maiden Pharmaceuticals sản xuất và xuất khẩu. Động thái này được đưa ra sau khi Tổ chức Y tế Thế giới (WHO) cảnh báo sản phẩm của họ liên quan cái chết của hàng chục trẻ em ở Gambia, theo Reuters.
Cái chết của 66 trẻ em ở quốc gia Tây Phi là đòn giáng mạnh vào hình ảnh "nhà thuốc lớn nhất thế giới" của Ấn Độ. Đất nước này chuyên cung cấp thuốc cho tất cả châu lục, đặc biệt châu Phi.
Ngày 6/10, WHO cho biết phân tích trong phòng thí nghiệm đối với 4 sản phẩm siro của Maiden, gồm Promethazine Oral Solution, Kofexmalin Baby Cough Syrup, Makoff Baby Cough Syrup và Magrip N Cold Syrup, đã xác nhận lượng diethylene glycol và ethylene glycol có thể gây độc. Đặc biệt, lượng chì "không thể chấp nhận được", có thể gây tổn thương thận cấp tính.
Diethylene glycol, ethylene glycol được sử dụng trong chất chống đông, chất lỏng phanh và các ứng dụng công nghiệp khác. Song, nó cũng là chất thay thế rẻ tiền trong một số sản phẩm dược phẩm.
Bộ Y tế Ấn Độ cho biết các mẫu của 4 loại siro trong cùng một lô do Maiden sản xuất đã được gửi đến phòng thí nghiệm liên bang kiểm tra. Cơ quan này sẽ "hướng dẫn hành động tiếp theo cũng như mang lại sự rõ ràng về các thông tin đã/sẽ nhận được từ WHO". Bộ cũng yêu cầu WHO chia sẻ báo cáo về mối quan hệ nhân quả giữa 4 loại siro này và nguy cơ tử vong.
Anil Vij, Bộ trưởng Y tế của bang Haryana, nơi Maiden đặt nhà máy, cảnh báo sẽ "hành động nghiêm khắc nếu phát hiện ra bất cứ sai sót gì" sau khi kiểm tra. Naresh Kumar Goyal, Giám đốc của Maiden, cho biết họ đã nghe về những ca tử vong khi uống siro ho và đang tìm hiểu thông tin.
“Chúng tôi đang cố gắng tìm hiểu tình hình vì nó mới chỉ xảy ra hôm qua. Sản phẩm này chỉ được xuất khẩu và không bán ở Ấn Độ", vị này nói.
 |
| Một người quay phim chụp ảnh bên ngoài văn phòng của công ty Maiden Pharmaceuticals Ltd., ở New Delhi, Ấn Độ, ngày 6/10. Ảnh: Reuters/Anushree Fadnavis. |
Ngày 5/10, Tổng giám đốc WHO Tedros Adhanom Ghebreyesus cho biết WHO đang điều tra các trường hợp tử vong do tổn thương thận cấp tính với cơ quan quản lý thuốc và nhà sản xuất thuốc của Ấn Độ.
WHO đã thông báo cho Tổng kiểm soát dược phẩm của Ấn Độ về những ca tử vong vào cuối tháng 9. Sau đó, cơ quan quản lý mở cuộc điều tra song song với WHO và giới chức Ấn Độ.
“Cho đến nay, nhà sản xuất đã không cung cấp bằng chứng đảm bảo an toàn và chất lượng của các sản phẩm này cho WHO”, cảnh báo cho biết. Phân tích trong phòng thí nghiệm các mẫu sản phẩm “xác nhận chúng chứa một lượng không thể chấp nhận được diethylene glycol và ethylene glycol như là chất gây hại”.
Những chất này có hại đối với con người và có thể gây tử vong. Các triệu chứng nhiễm độc các chất này “có thể bao gồm đau bụng, nôn mửa, tiêu chảy, khó tiểu, đau đầu, trạng thái tinh thần thay đổi liên tục và tổn thương thận cấp tính, có thể dẫn đến tử vong”.
WHO cho biết thông tin nhận được từ Tổ chức Kiểm soát Tiêu chuẩn Thuốc Trung ương của Ấn Độ chỉ ra nhà sản xuất chỉ cung cấp thuốc bị nhiễm độc cho Gambia.
Hôm 6/10, chính quyền Gambia đã bắt đầu thu hồi siro có chứa paracetamol và promethazine từ các hộ gia đình nông thôn ở một số vùng. Cơ quan y tế cũng đã ra lệnh thu hồi vào ngày 23/9 tất cả các loại thuốc có chứa paracetamol hoặc promethazine.
Công ty Maiden bắt đầu hoạt động vào tháng 11/1990, chỉ sản xuất và xuất khẩu siro sang Gambia, Bộ Y tế Ấn Độ cho biết. Trên website của mình, Maiden cho biết họ có 2 nhà máy sản xuất, ở Kundli và Panipat, cả hai đều gần New Delhi. Gần đây, họ xây dựng thêm một nhà máy khác.
Nhà máy của Maiden có công suất sản xuất hàng năm là 2,2 triệu chai siro, 600 triệu viên nang, 18 triệu liều thuốc tiêm, 300.000 ống thuốc mỡ và 1,2 tỷ viên nén. Trên website công ty này cho biết bán sản phẩm trong nước và xuất khẩu sang các nước ở châu Á, châu Phi và châu Mỹ Latin, mặc dù ông Goyal khẳng định họ hiện không bán ở Ấn Độ.
Bộ Y tế Ấn Độ cho biết các nước nhập khẩu thường kiểm tra các sản phẩm trước khi cho phép sử dụng.


