Trước thông tin Việt Nam sắp có vắc xin sốt xuất huyết (SXH), TS Nguyễn Ngô Quang - Phó cục trưởng Cục Khoa học Đào tạo, Bộ Y tế - cho hay Việt Nam chỉ là một trong các trung tâm nghiên cứu, không phải là địa điểm nghiên cứu và thử nghiệm duy nhất loại vắc xin này.
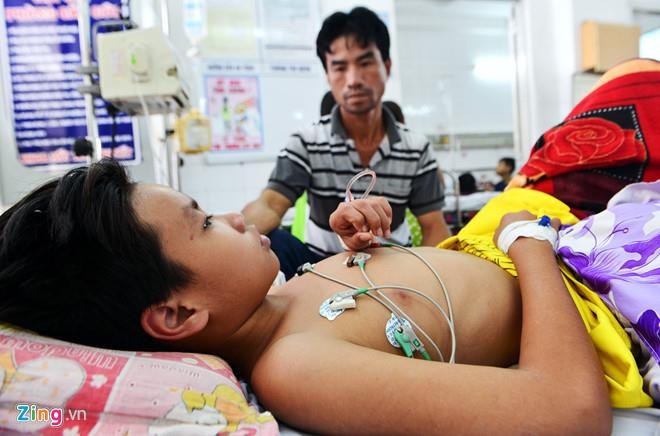 |
| Bệnh nhi bị sốt xuất huyết đang điều trị tại Bệnh viện Nhi Đồng 1. Ảnh: Lê Quân. |
Cụ thể, vắc xin SXH Dengvaxia của Sanofi Pasteur bắt đầu nghiên cứu cách đây hơn 20 năm. Vắc xin này trải qua nhiều giai đoạn nghiên cứu trên động vật và trên người, về dược lý, tính an toàn, hiệu quả.
Từ năm 2011-2017, hai nghiên cứu lớn về tính an toàn và hiệu quả của vắc xin này được thực hiện và hoàn thành ở 10 quốc gia, trong đó có Việt Nam.
Trên kết quả nghiên cứu này, công ty Sanofi Pasteur đã đăng ký lưu hành Dengvaxia ở nhiều nước trên thế giới. Vắc xin này chỉ định để phòng chống bệnh SXH do 4 type huyết thanh của virus SXH gây ra. Tính đến nay, có 54 quốc gia trên thế giới cấp phép cho lưu hành vắc xin Dengvaxia như Mỹ, Pháp, Thụy Điển, Thái Lan,…
Ở nước ta, nhóm nghiên cứu của Viện Pasteur TP.HCM được giao thực hiện nghiên cứu từ năm 2011. PGS.TS Trần Ngọc Hữu, nguyên Viện trưởng Viện Pasteur TP.HCM, Chủ nhiệm đề tài nghiên cứu vắc xin SXH, cho biết việc nghiên cứu vắc xin SXH Dengvaxia tại Việt Nam đã hoàn tất.
“Ở Việt Nam, toàn bộ trẻ tham gia nghiên cứu và thử nghiệm vắc xin đều an toàn, không xảy ra tai biến”, ông Hữu cho hay.
Sốt xuất huyết (SXH) là bệnh truyền nhiễm, dễ bùng phát thành dịch với diễn biến phức tạp ở nước ta. Bệnh chưa có thuốc trị đặc hiệu cũng như vắc xin phòng chống bệnh. Cách duy nhất là tránh bị muỗi đốt - con đường khiến bệnh lây truyền. Việc có vắc xin SXH được xem là tin vui để chống lại căn bệnh này.
Tuy nhiên, theo TS Quang, kết quả nghiên cứu này cần có đánh giá nghiệm thu. Hiện nay, nhóm nghiên cứu đang tiến hành tổng hợp lại toàn bộ dữ liệu để báo cáo Bộ Y tế.
Sau đó, Bộ Y tế sẽ thành lập Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia để đánh giá, nghiệm thu kết quả. Tuy nhiên, kết quả ở Việt Nam chỉ là một phần trong kết quả chung trên toàn cầu gồm nhiều các quốc gia khác. Từ những kết quả tại các quốc gia khác nhau, nhà sản xuất sẽ tổng hợp, sau đó, các cơ quan quản lý về dược phẩm, đặc biệt là các cơ quan quản lý về vắc xin mới quyết định cho phép sử dụng hay không.
“Chúng ta phải chờ đợi kết quả từ các trung tâm khác mới có thể đánh giá được toàn diện về loại vắc xin này. Đơn vị nghiên cứu phải đăng ký với cơ quan quản lý ở Việt Nam nếu muốn đăng ký lưu hành ở Việt Nam”, TS Quang nhấn mạnh.
Về giá của loại vắc xin này, ông Quang cho hay: “Hiện tại, giá cả lưu hành tại Việt Nam của vắc xin này tôi không nắm được, mà Sanofi Pasteur sẽ đưa ra. Tuy nhiên, nếu được cấp phép lưu hành ở Việt Nam, tôi nghĩ Sanofi Pasteur sẽ ưu tiên cung ứng vắc xin SXH với giá cả hợp lý nhất”.