Thời gian gần đây, nhiều tờ báo đưa tin: "Đã tìm ra cách tiêu diệt mọi loại ung thư?” hoặc “Tạo ra virus tiêu diệt mọi loại tế bào ung thư”. Nội dung này liên quan đến phương pháp điều trị ung thư sử dụng virus đậu mùa có tên CF33 đã có nhiều thành công trong các nghiên cứu tiền lâm sàng và đang hướng đến thử nghiệm lâm sàng (trên người) trong thời gian tới đây.
Bài viết dưới đây của TS Nguyễn Hồng Vũ, Viện nghiên cứu City of Hope, California, Mỹ, Cố vấn khoa học Ruy Băng Tím, sẽ phân tích về phương pháp này.
Trong những thập niên gần đây, việc sử dụng virus trong điều trị ung thư đang được nghiên cứu nhiều hơn. Các virus này được biết đến như oncolytic virus (Onco có nghĩa là “ung thư”, lytic có nghĩa “tiêu hủy”). Chúng có khả năng lây nhiễm và tiêu diệt tế bào khối u. Các loại virus này được tìm thấy ở tự nhiên hoặc biến đổi trong phòng thí nghiệm để đảm bảo an toàn, tăng hiệu quả việc lây nhiễm, sinh sản, độc lực một cách “đặc hiệu” ở các tế bào ung thư mà không gây hại cho tế bào khỏe mạnh.
Ngoài tiêu diệt tế bào trực tiếp, một cơ chế khác của oncolytic virus cũng quan trọng không kém là khi tế bào ung thư sắp chết hoặc chết bởi virus sẽ giải phóng vật liệu trong tế bào được biết như kháng nguyên khối u. Chúng cho phép các tế bào ung thư được nhận ra hoặc nhìn thấy bởi tế bào miễn dịch. Sau đó, các tế bào miễn dịch sẽ tấn công và tiêu diệt tế bào ung thư hiệu quả hơn.
Lịch sử ghi nhận khá nhiều nghiên cứu về sử dụng virus để điều trị ung thư với các thế mạnh và tiềm năng khác nhau trong giai đoạn tiền lâm sàng và thử nghiệm lâm sàng. Tuy nhiên, cho đến hiện nay, chỉ có một loại được Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) phê duyệt cho sử dụng trên người là herpesvirus được biến đổi gen có tên Talimogene Laherparepvec (T-Vec, hay tên thương mại là Imlygic) để điều trị ung thư hắc tố (Melanoma).
 |
| GS Yuman Fong cho biết phương pháp mới đã có tác dụng trên chuột thí nghiệm. Ảnh: News360. |
CF33 được tạo ra như thế nào?
Để tạo ra CF33, các nhà khoa học đã cho nhiễm nhiều chủng virus được biết trước đó thuộc nhóm orthopoxvirus vào tế bào CV-1 (African green monkey kidney fibroblasts, tế bào thận của khỉ) để các chủng virus này tự tái tổ hợp với nhau. Sau đó, từ tế bào nhiễm họ chọn lọc và tinh sạch 100 chủng virus khác nhau.
Các chủng virus này được sàng lọc trên một nhóm gồm 60 dòng tế bào ung thư ở người của Viện Ung thư Quốc gia (National Cancer Institute - NCI) để chọn ra dòng virus có tác dụng tiêu diệt tế bào ung thư mạnh. Qua quá trình này, họ chọn lọc ra dòng virus có tên CF33. Từ virus CF33 cơ bản này, nhóm tác giả cũng thay đổi một số điểm để tạo ra các “dị bản” của CF33 như CF33-Fluc, CF33-GFP, CF33-hNIS.
Các thành công của CF33 trong các nghiên cứu tiền lâm sàng
Năm 2018, nhóm các nhà khoa học này đã có một công trình đăng trên tạp chí chuyên ngành Journal of Translational Medicine. Trong đó, họ sử dụng virus CF33 để điều trị ung thư ung thư tụy ở chuột. Tế bào ung thư tụy của người (tên các dòng tế bào là PANC-1 và MIA PACA-2) được chích dưới da chuột để tạo khối u và sau đó virus được chích trực tiếp vào khối u để quan sát hiệu quả điều trị. Kết quả cho thấy chúng có khả năng làm chậm sự phát triển của khối u, thậm chí làm khối u nhỏ lại so với nhóm đối chứng.
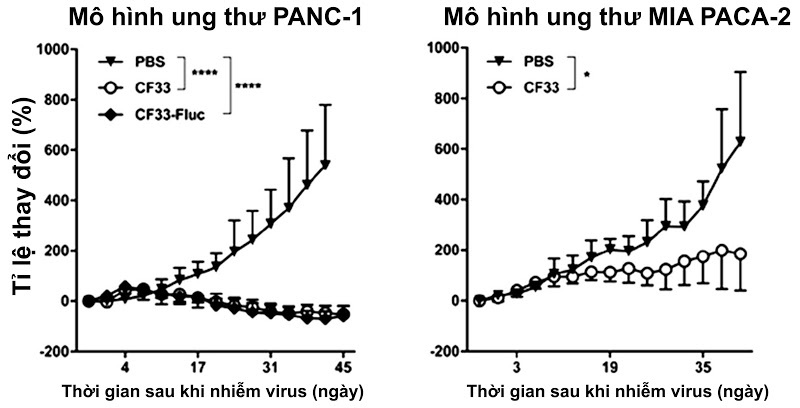 |
| Hiệu quả điều trị của virus CF33 trên mô hình ung thư tụy. Ảnh: NVCC. |
Trong năm 2019, họ có công bố 2 công trình nghiên cứu khác cũng sử dụng virus CF33 nhưng có một số biến đổi. Công trình đăng trên tạp chí Cancer Gene Therapy sử dụng chủng virus CF33 bị đột biến bất hoạt gene tạo enzyme thymidine kinase và gắn gene GFP (virus có tên là CF33-GFP). Trong thí nghiệm này, họ sử dụng mô hình ung thư phổi tạo dưới da chuột. Kết quả cho thấy hiệu quả kìm hãm khối u của virus khá mạnh ở dòng tế bào A549 và yếu hơn ở dòng tế bào LLC1.
Một công trình khác công bố trong cùng năm đăng trên tạp chí Molecular Therapy Oncolytics sử dụng chủng virus CF33 được gắn thêm gene tạo kênh đồng vận chuyển Natri-iốt (Symporter Natri-Iodide) của người (hNIS) để giúp theo dõi virus trong cơ thể, cũng như kết hợp xạ trị trúng đích (virus có tên là CF33-hNIS).
Trong công trình này, họ sử dụng mô hình ung thư đại tràng tạo dưới da chuột. Kết quả cho thấy, nhờ vào hoạt động của gene hNIS mà họ có thể quan sát được vị trí của virus bằng máy PET/CT khi sử dụng đồng vị phóng xạ để định vị. Ngoài ra, việc kết hợp đồng vị phóng xạ với virus đã tăng hiệu quả điều trị ung thư lên rất nhiều.
Việc phát triển phương pháp này đang đi tới đâu?
Hiện nay, công ty công nghệ sinh học của Australia là Imugene đang phối hợp với nhóm nghiên cứu này (có thể họ sẽ mua bản quyền) để chuẩn bị cho giai đoạn thử nghiệm lâm sàng của CF33 trong năm tới.
Do thử nghiệm lâm sàng vẫn chưa được bắt đầu và tuyển tình nguyện viên thử thuốc nên nội dung thử nghiệm cụ thể như thế nào vẫn chưa được biết. Tuy nhiên, nhiều khả năng họ sẽ thử trên các bệnh nhân có loại ung thư đã có những thử nghiệm thành công ở chuột trong giai đoạn tiền lâm sàng như ung thư tụy, ung thư phổi, ung thư đại tràng và ung thư vú (thành công trên chủng virus CF189).
Theo tài liệu của công ty Imugene, kế hoạch thử nghiệm lâm sàng của họ sẽ khái quát như hình sau:
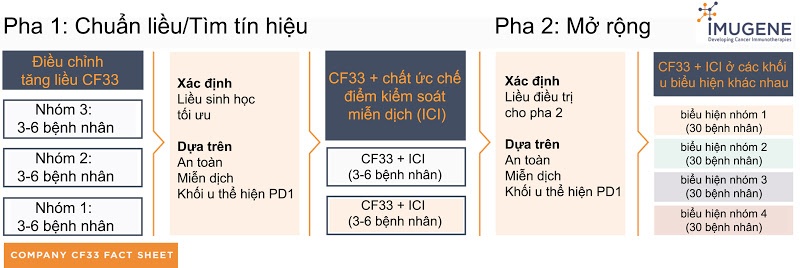 |
| Thông tin về dự thảo thử nghiệm lâm sàng CF33 của công ty IMUGENE. Ảnh: NVCC. |
Các thành công ban đầu chỉ mới trên mô hình khối ung thư ở da (subcutaneous) chuột. Tuy nhiên, các kết quả khả quan trong giai đoạn tiền lâm sàng của CF33 cho chúng ta hy vọng. Con đường phát triển thuốc này còn dài và nhiều chông gai phía trước.
Ruy Băng Tím là tổ chức phi lợi nhuận về phòng chống ung thư tại Việt Nam, được thành lập vào ngày 12/12/2015 với sự tham gia của các bác sĩ ung bướu, các nhà khoa học nghiên cứu về ung thư trong và ngoài nước.
Tài liệu tham khảo:
- Sivanandam V, LaRocca CJ, Chen NG, Fong Y, Warner SG, 2019. Oncolytic Viruses and Immune Checkpoint Inhibition: The Best of Both Worlds. Mol Ther Oncolytics. 13:93-106.
- O'Leary MP, 2018. Novel oncolytic chimeric orthopoxvirus causes regression of pancreatic cancer xenografts and exhibits abscopal effect at a single low dose. J Transl Med. 16:110.
- Chaurasiya S, 2019. A chimeric poxvirus with J2R (thymidine kinase) deletion shows safety and anti-tumor activity in lung cancer models. Cancer Gene Ther. doi: 10.1038/s41417-019-0114-x.
- Warner SG et al., 2019. A Novel Chimeric Poxvirus Encoding hNIS Is Tumor-Tropic, Imageable, and Synergistic with Radioiodine to Sustain Colon Cancer Regression. Mol Ther Oncolytics. 13:82-92.
- Choi AH, 2018. Novel chimeric parapoxvirus CF189 as an oncolytic immunotherapy in triple-negative breast cancer. Surgery. 163:336-342.
- https://static1.squarespace.com/static/5b63d41b3e2d09b1f56bf483/t/5d2bae446bef550001e2c927/1563143751349/Oncolytic+Cancer+Virus+Fact+Sheet+.pdf


